Weitere Mechanismen bei der Entstehung von Leukämien aufgeklärt
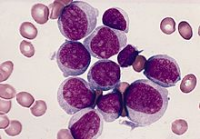
Jena (UKJ/vdG) – Sowohl bei der Akuten als auch bei der Chronischen Myeloischen Leukämie führt die vermehrte Produktion reaktiver Sauerstoffspezies in den Tumorzellen zu einem Fortschreiten der Erkrankung. Wissenschaftler des Universitätsklinikums Jena (UKJ) konnten diese Wirkmechanismen aufklären. Ihre jüngst im Fachjournal BLOOD veröffentlichten Ergebnisse sprechen dafür, dass die Herabsetzung der Produktion solcher Sauerstoffspezies in Leukämie-Zellen ein mögliches neues therapeutisches Prinzip ist.
Neuere Studien zeigen durchaus auch positive Seiten der sogenannten reaktiven Sauerstoffspezies, kurz ROS, auf: Wenn sie zum Beispiel als Trainingssystem für Abwehrmechanismen gegen oxidativen Stress in der Zelle dienen oder bei Signalübertragungsprozessen mitwirken. Zuviel dieser aggressiven Formen des Sauerstoffs, oft ungenau als Sauerstoffradikale bezeichnet, ist aber eindeutig schädlich und spielt bei Alterungsprozessen oder der Entstehung von Arteriosklerose und Alzheimer eine Rolle. Auch in verschiedenen Typen von Tumorzellen ist die Produktion von ROS erhöht.
Die molekularen Ursachen für dieses Phänomen und die Rolle, die ROS in Tumorerkrankungen spielen, sind jedoch bisher nur in Ansätzen verstanden“, so Prof. Dr. Andreas Hochhaus. Der Hämatologe leitet das UniversitätsTumorCentrum am Jenaer Uniklinikum, dessen Wissenschaftler jetzt in zwei Studien zur Aufklärung der molekularen Wirkmechanismen von ROS in den Zellen zweier Leukämieformen beitragen konnten.
AML: ROS stört Regulierung der Zellteilung
In Zellen der Akuten Myeloischen Leukämie AML, in denen ein Onkoprotein die ungebremste Teilung der Zellen antreibt, werden große Mengen an ROS gebildet. „Wir konnten zeigen, dass diese ROS-Moleküle die Inaktivierung eines anderen Enzyms bewirken, das normalerweise als ‚Bremse’ der Zellteilung funktioniert“, beschreibt Prof. Frank-D. Böhmer vom Institut für Molekulare Zellbiologie ein Ergebnis seiner Arbeitsgruppe. Wird die krankhafte ROS-Produktion in den Zellen experimentell unterbrochen, so wird dieses Enzym wieder aktiv und die Vermehrung der Leukämiezellen verlangsamt sich.
CML: ROS lässt Leukämiezellen resistent werden
Fatale Wirkungen, so das Ergebnis einer weiteren internationalen Studie, hat ROS auch bei einer anderen Form der Leukämie, der Chronischen Myeloischen Leukämie CML. Seit einigen Jahren ist diese genetisch bedingte Krebserkrankung des blutbildenden Systems mit spezifischen Wirkstoffen behandelbar, die sich gegen ein Onkoprotein in den Leukämiezellen richten und diese absterben lässt. In den Mitochondrien, den Kraftwerken der verbleibenden CML-Zellen und vor allem in den Leukämiestammzellen werden aber als „Nebenprodukt“ weiterhin verstärkt ROS gebildet, die Schäden am Erbgut verursachen können. „Diese Schäden können auch das Krebsgen so verändern, dass die Leukämiezellen unempfindlich werden gegen den Wirkstoff und ihre Zahl wieder anwächst“, erklärt Andreas Hochhaus, der an der Studie beteiligt war.
„Die Ergebnisse beider Studien sprechen dafür, dass die Verminderung der Produktion reaktiver Sauerstoffspezies in Leukämie-Zellen ein neues therapeutisches Prinzip bei myeloischen Leukämien sein könnte“, geben die Jenaer Wissenschaftler einen Ausblick auf die klinische Anwendung ihrer Ergebnisse.
Originalliteratur:
Godfrey R, et al. Cell transformation by FLT3 ITD in acute myeloid leukemia involves oxidative inactivation of the tumor suppressor protein-tyrosine phosphatase DEP-1/PTPRJ. Blood. 2012 Mar 20. [Epub ahead of print]
Nieborowska-Skorska M, et al. Rac2-mitochondrial respiratory chain complex III-generated ROS cause genomic instability in chronic myeloid leukemia stem cells and primitive progenitors. Blood. 2012 Mar 12. [Epub ahead of print]
(Pressemitteilung des Universitätsklinikums Jena)
